

发布时间:2026-04-17
我做转录组测序,发现基因X的mRNA水平上调了10倍,高高兴兴跑去跑了个WB,结果蛋白条带怎么没啥变化?是不是抗体有问题?还是我操作翻车了?
先别急着怀疑人生,也别急着甩锅给抗体。这很可能不是你的错,而是你在用“尺子量体重”——用错了工具!
今天我们就来掰扯掰扯:为什么WB通常不直接用来验证转录组结果? 看完你就明白,这背后藏着细胞生物学最核心的“游戏规则”。
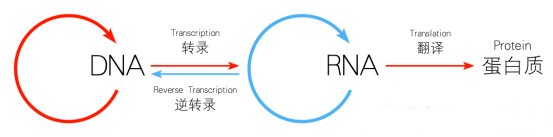
先打个比方:
转录组(mRNA) 像是你手机里的购物车——里面加购了很多商品,代表你“打算”要买什么。
蛋白质 像是你实际收到快递、拆开用上的东西——这才是真正发挥功能的“最终产品”。
购物车里的东西(mRNA)多,不代表你最后收到的快递(蛋白)就一定多。为什么?
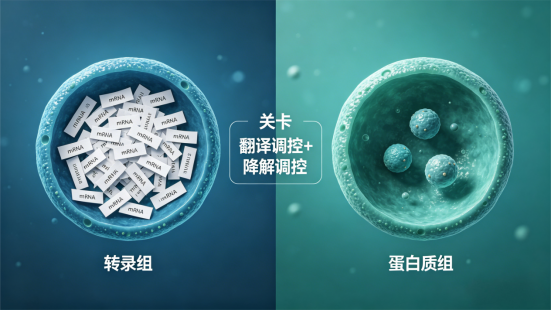
因为从mRNA到蛋白,中间隔着两大“变数”:

这不是我瞎说的,顶级期刊早就报道过:
多项系统生物学研究表明,mRNA与对应蛋白表达水平的相关系数通常在0.4~0.6之间,属于中等相关,远不是1:1的线性关系。
也就是说,mRNA涨了10倍,蛋白可能只涨了1.5倍,甚至压根不涨。
真实案例:
很多炎症因子、趋化因子,转录水平可以在刺激后飙升几十倍,但分泌到胞外的蛋白水平可能只增加2-3倍——因为翻译后修饰、分泌效率、胞外降解都在“调控”最终结果。
所以,如果你用WB去“验证”转录组的倍数变化,大概率会“翻车”。这不是WB不行,而是它们俩问的是两个不同的问题。
那WB到底适合干什么?记住这三条,以后不迷茫:
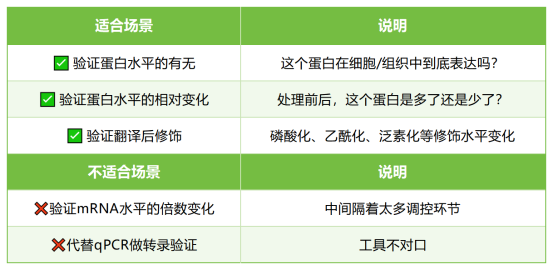
简单总结:
想验证mRNA变化?→ 做qPCR
想验证蛋白变化?→ 做WB
别拿WB去“复核”转录组的结果,除非你先确认了该基因的mRNA-蛋白相关性在你这套体系里是好的。
转录组发现某个基因mRNA变了,接下来正确的“科学姿势”是这样的:
第一步:qPCR验证(在同一批样品中重复确认mRNA变化)
第二步:看蛋白(可选,取决于你的科学问题)
如果你关心的是功能执行者(蛋白),那值得做WB
但要有心理准备:趋势可能一致,但倍数可能对不上
第三步:功能性实验(敲低/过表达/抑制剂,看表型)
重点:如果WB结果和转录组趋势不一致,这不叫“验证失败”,这叫发现了一个新的调控机制——比如转录后调控、翻译抑制、蛋白降解加速。这反而可能是一个不错的发表点!
说了这么多,并不是说WB不好。恰恰相反,WB仍然是检测蛋白表达的金标准——前提是你要在它擅长的领域使用它。
而WB实验成败的关键,很大程度取决于抗体的质量。
一条清晰的特异性条带,可以让你自信地得出结论;而一条背景脏、杂带多的膜,只会让你在审稿人面前百口莫辩。
这时候,你需要一位靠谱的“战友”——优品生物。
优品生物的高品质WB抗体,采用高纯度制备工艺,为你保驾护航:
✔ 高特异性——条带清晰,背景干净,帮你彻底告别非特异性条带的困扰,让WB数据更有说服力
✔ 高稳定性——4℃保存时间长,即便反复回收利用,信号衰减也极慢,抗体的耐用性超乎你想象
✔ 多种包装规格——担心用不完浪费?我们提供小包装(如10μL试用装),先试后买,为实验室的每一分经费负责
✔ 覆盖全面——无论是看家基因的内参,还是磷酸化修饰,甚至是那些罕见的“冷门”靶点,优品生物一应俱全
下次别再拿WB去“硬刚”转录组的结果了——工具用对,事半功倍;工具用错,怀疑人生。
而当你真正需要讲好“蛋白的故事”时,优品抗体,随时待命。