
发布时间:2026-04-24
摘要:
背景: 压力性溃疡常见于卧床老年人群,死亡率高且缺乏有效治疗手段。本研究开发了人脂肪来源干细胞-透明质酸凝胶(hADSCs-HA凝胶),并通过体内外实验研究其疗效及旁分泌机制。
方法: 在C57BL/6小鼠背部建立压力性溃疡模型,分别局部给予hADSCs-HA凝胶、hADSCs、透明质酸(HA)和生理盐水。连续观察14天伤口闭合率,并取伤口组织进行Western blot、组织病理学、免疫组织化学及蛋白质组学分析。在正常或低氧条件下,用人ADSCs条件培养基(ADSC-CM)处理人真皮成纤维细胞(HDFs)和人脐静脉内皮细胞(HUVECs),通过CCK-8、划痕实验、管形成实验及Western blot评估hADSCs的旁分泌效应及其机制。
结果: 体内实验表明,hADSCs-HA凝胶通过促进胶原表达、血管生成和皮肤增殖,显著加速压力性溃疡愈合。体外实验显示,hADSCs通过旁分泌方式增强HDFs和HUVECs的增殖与伤口愈合能力,同时促进胶原分泌和管形成。ADSC-CM对低氧状态下的HDFs和HUVECs也具有保护作用。蛋白质组学及Western blot结果阐明,脂质代谢和PPARβ/δ通路介导了hADSCs-HA凝胶对压力性溃疡的愈合作用。
结论: 局部应用hADSCs-HA凝胶在真皮再生和血管生成中发挥重要作用,具有作为新型干细胞治疗策略在临床治疗压力性溃疡中的潜力。
关键词: 压力性溃疡,伤口愈合,人脂肪来源干细胞,水凝胶,PPARβ/δ,脂质代谢,皮肤再生
核心内容:
体内实验:
hADSCs-HA凝胶组在第14天伤口闭合率达96.91%,显著高于HA组(88.20%)和hADSCs组(86.72%)。
HE染色显示,模型组表皮坏死、炎性细胞浸润明显;hADSCs-HA组表皮再生良好,炎性渗出减少。
Masson染色显示hADSCs-HA组胶原面积分数显著升高。
免疫组化和Western blot显示,hADSCs-HA组Col-1、Col-3、CD31、PCNA表达均显著高于其他组。
与胶原凝胶对照组相比,hADSCs-HA组各项指标也显著更优。
体外实验:
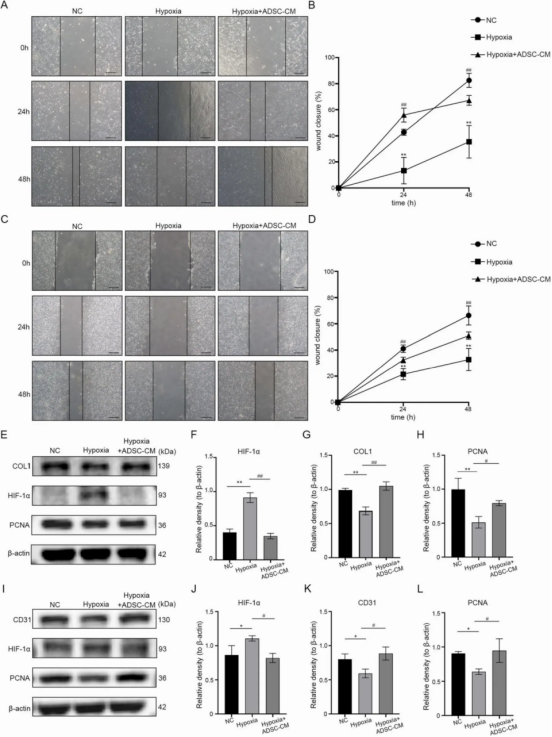
ADSC-CM显著促进HDFs和HUVECs的增殖、迁移及HDFs的胶原合成。
ADSC-CM显著增强HUVECs的管形成能力(分支点数和总管长度增加)。
在低氧条件下,ADSC-CM降低HIF-1α表达,恢复HDFs和HUVECs的增殖、胶原合成(HDFs)和CD31表达(HUVECs)。
ADSC-CM上调HDFs和HUVECs中PPARβ/δ及下游ANGPTL4的表达。
GSK3787可阻断ADSC-CM对Col-1、PCNA(HDFs)和CD31(HUVECs)的促进作用,证实PPARβ/δ通路的关键介导作用。
蛋白质组学:
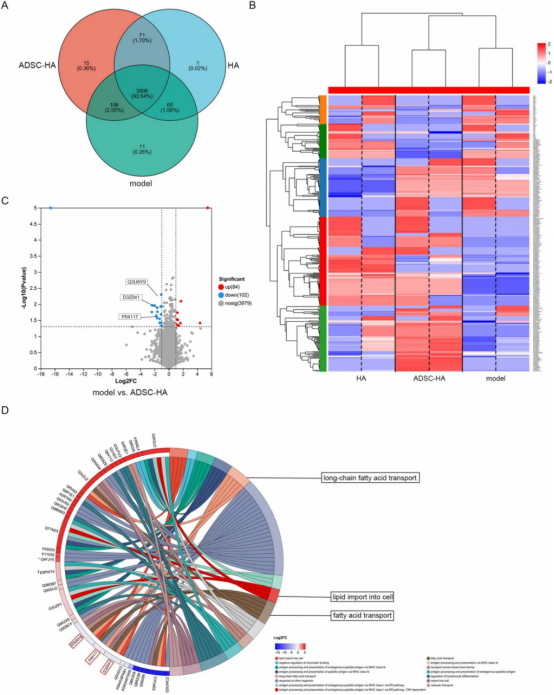
ADSC-HA组与模型组相比,差异表达蛋白富集于“脂肪酸转运”“长链脂肪酸转运”“脂质进入细胞”等GO条目。
KEGG分析显示PPARβ/δ信号通路、脂肪细胞因子信号通路、脂肪酸降解通路显著富集,其中PPARβ/δ通路最为显著。
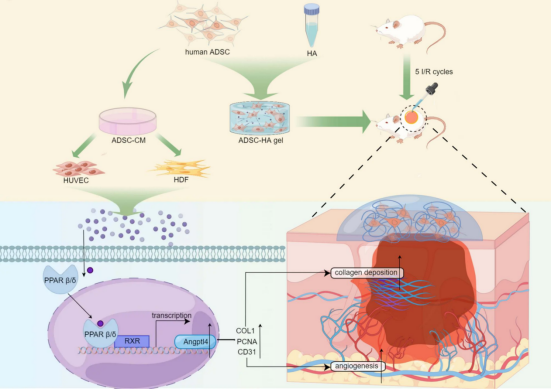
动物模型建立:
使用C57BL/6小鼠,背部皮肤通过磁铁压迫-再灌注循环(12小时压迫+12小时休息,共4个周期)建立压力性溃疡模型。
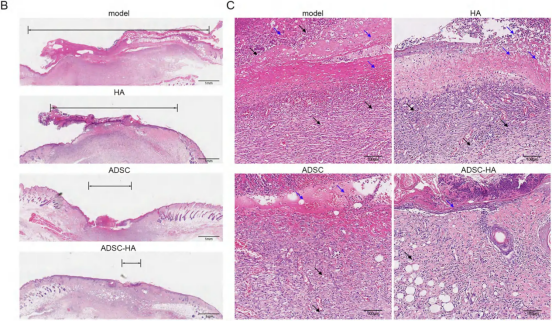
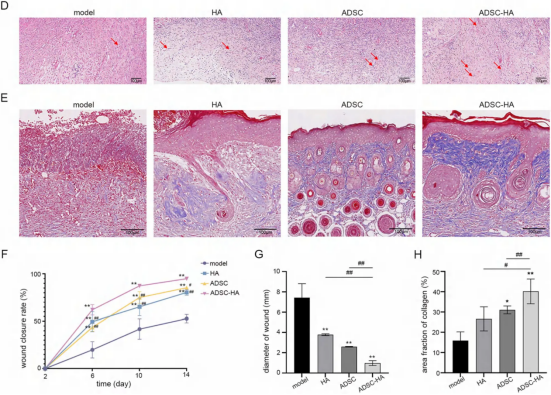
实验分组:
模型组(生理盐水)、HA组、hADSCs组、hADSCs-HA组,每组8只小鼠。另设胶原凝胶对照组。
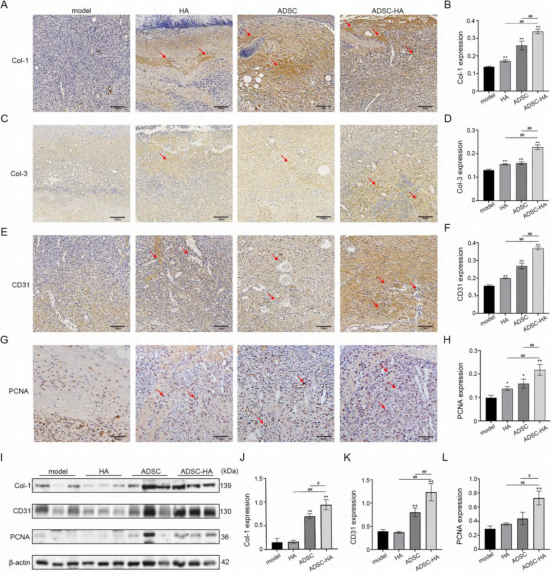
细胞培养与条件培养基制备:
hADSCs、HDFs、HUVECs分别培养于相应培养基。
ADSC-CM:hADSCs在DMEM+10% FBS中培养48小时收集上清。
低氧模型:使用100 μM CoCl₂模拟低氧环境。
检测指标:
体内:伤口闭合率、HE染色、Masson染色、免疫组化(Col-1、Col-3、CD31、PCNA)、Western blot(Col-1、CD31、PCNA)。
体外:CCK-8(增殖)、划痕实验(迁移)、管形成实验(HUVECs)、Western blot(PCNA、Col-1、Col-3、CD31、HIF-1α、PPARβ/δ、ANGPTL4)。
蛋白质组学:鉴定差异表达蛋白,GO和KEGG富集分析。
机制验证:
使用PPARβ/δ特异性抑制剂GSK3787,验证ADSC-CM对HDFs和HUVECs的作用是否依赖该通路。
讨论与总结要点:
创新性:
本研究首次采用局部涂抹hADSCs-HA凝胶治疗压力性溃疡,避免注射或手术创伤,提高临床应用安全性。
证实hADSCs通过旁分泌方式(而非直接分化)发挥促愈合作用,尤其在低氧环境下仍能保护HDFs和HUVECs。
明确PPARβ/δ-ANGPTL4轴是介导hADSCs促愈合效应的关键分子通路。
机制阐释:
hADSCs通过旁分泌激活PPARβ/δ通路,上调ANGPTL4、PCNA、Col-1、CD31等蛋白,促进成纤维细胞增殖、胶原合成及内皮细胞血管形成。
PPARβ/δ作为脂质代谢与组织再生的桥梁,可能在低氧条件下通过改善线粒体功能、减少氧化应激和内质网应激,保护细胞免受损伤。
优势与前景:
hADSCs-HA凝胶制备简便、生物相容性好、免疫原性低,优于其他水凝胶支架。
除压力性溃疡外,也具备治疗糖尿病溃疡、烧伤、放射性损伤的潜力。
局限性:
hADSCs质量受供体因素影响,需加强质控;
凝胶的储存条件尚需优化;
生物相容性及长期安全性需进一步研究。
1、质量控制:建立hADSCs的标准化制备流程,减少供体个体差异对疗效的影响。
2、储存条件:优化hADSCs-HA凝胶的储存方法(如温度、期限),便于临床推广。
3、生物相容性与安全性:深入评估凝胶的长期生物相容性及免疫原性。
4、机制深化:探索PPARβ/δ通路与自噬、氧化应激、线粒体功能等其他机制的交叉调控关系。
5、适应症拓展:验证该凝胶在糖尿病溃疡、烧伤、放射性皮肤损伤等其他难愈性创面中的疗效。
文献推荐
IF 4.7

YP-Ab-16944anti-CD31 antibody