
发布时间:2026-03-27
摘要
目的:酒精性肝病(ALD)是肝细胞癌的病因之一,并伴随肠道渗漏和微生物群变化。葛根对肝损伤具有保护作用。本研究旨在探讨葛根治疗ALD的机制。采用超高效液相色谱-四极杆飞行时间质谱(UPLC-Q/TOF-MS)分析葛根提取物(PUE)的成分。
方法:通过建立急性和慢性ALD模型,评估PUE的抗酒精和保肝效果。结果显示,PUE治疗降低了血清中丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、总胆固醇(TC)和甘油三酯(TG)的水平以及炎症因子水平,减轻了肝脏炎症和醉酒状态。PUE通过下调乙醇脱氢酶1(ADH1)的基因表达和血清乙醛(ACH)水平,抑制了乙醇代谢生成ACH,同时上调乙醛脱氢酶2(ALDH2)的基因水平以加速ACH分解,从而减轻肝脏炎症和肠道屏障损伤。同时,16S rDNA测序显示,PUE改变了微生物群组成,减少了变形菌门和脱硫杆菌门的丰度,从而抑制了脂多糖(LPS)的生成及其下游Toll样受体4(TLR4)/髓样分化因子88(MyD88)/核因子κB(NF-κB)通路。PUE还增加了拟杆菌属、瘤胃球菌属和普雷沃氏菌属的丰度,并产生短链脂肪酸(SCFAs)以保护肠壁。
结论:粪便微生物群移植(FMT)治疗进一步证实,PUE以肠道微生物群依赖的方式缓解ALD。因此,PUE通过调节肠道微生物群和抑制乙醇代谢,经由肝-肠-脑轴缓解ALD,未来具有良好的应用前景。
关键词:
酒精性肝病,肠道微生物群,野葛根,脂多糖,肝-肠-脑轴
核心内容
酒精性肝病(ALD)主要由长期或过量饮酒引起,可从酒精性肝炎、脂肪肝发展为肝纤维化、肝硬化甚至肝细胞癌。肝-肠-脑轴参与了ALD的形成。酒精在肝脏中代谢为乙醛(ACH),增加肠道通透性,破坏肠道菌群,使脂多糖(LPS)从肠腔转移至循环系统。随后,LPS与肝脏中的Toll样受体4(TLR4)结合,激活MyD88/NF-κB通路,上调促炎细胞因子水平,进一步加剧肝脏氧化损伤。同时,炎症因子和LPS通过迷走神经和血脑屏障进入大脑,引起神经炎症,导致运动迟缓、肢体无力及翻正反射丧失。葛根是一种药食同源植物,富含黄酮类、三萜类和多糖,对脑、肝、心和生殖系统有保护作用。目前,葛根治疗肝损伤的研究多集中于非酒精性肝病,对ALD的研究较少,且多集中于异黄酮和多糖等单体。由于肝-肠-脑轴的存在以及酒精对肠道和肝脏的共同损伤,葛根治疗ALD的机制尚不明确,有待充分阐明。
研究流程示例
葛根提取物(PUE)制备: 新鲜葛根用80%乙醇浸泡过夜,80℃提取2小时,上清液真空旋蒸干燥,得到PUE。
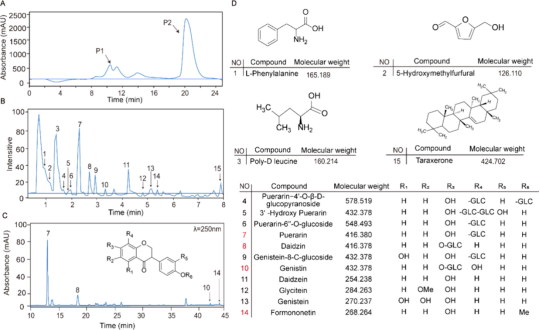
成分分析:
采用紫外-可见分光光度法(UV-Vis)测定PUE中总黄酮、总多糖、总多酚、总皂苷和总蛋白的含量。
采用高效凝胶渗透色谱(HPGPC)结合示差折光检测器(RID)分析多糖的分子量分布。
采用UPLC-Q/TOF-MS对PUE中的化合物进行定性分析。
采用高效液相色谱(HPLC)对四种典型异黄酮(葛根素、大豆苷、染料木苷和芒柄花素)进行定量分析。
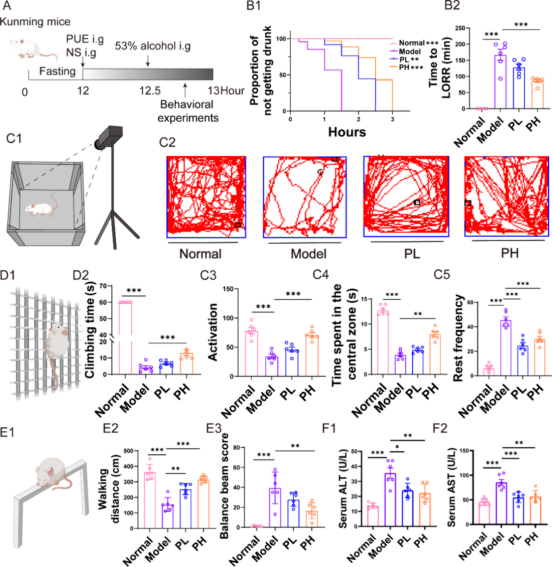
动物实验:
急性ALD模型: 小鼠连续3天灌胃PUE(低、高剂量)或生理盐水,末次给药30分钟后灌胃酒精,随后进行行为学测试(翻正反射、旷场、爬杆、平衡木)并检测血清ALT/AST水平。
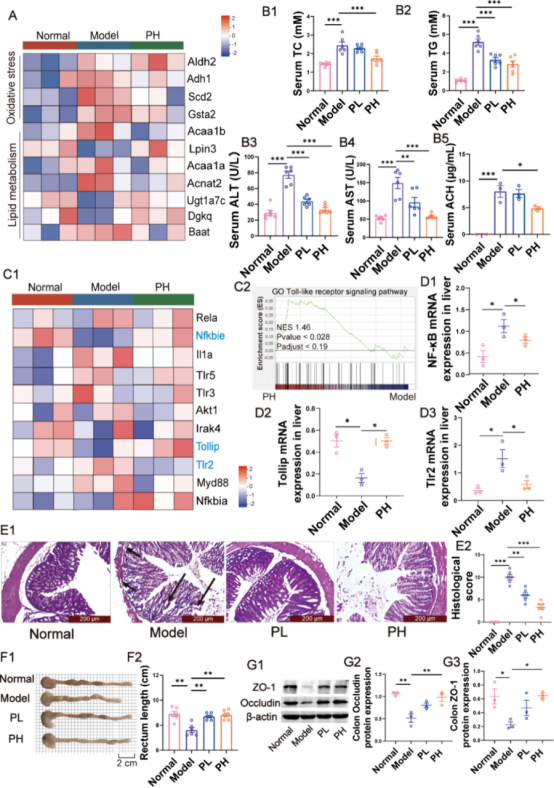
慢性ALD模型: 小鼠连续4周每天灌胃PUE或生理盐水,30分钟后灌胃酒精。收集血液、肝脏、回肠及内容物,进行生化指标检测、组织病理学分析、转录组测序、实时定量PCR(RT-PCR)、Western Blot和16S rDNA测序。
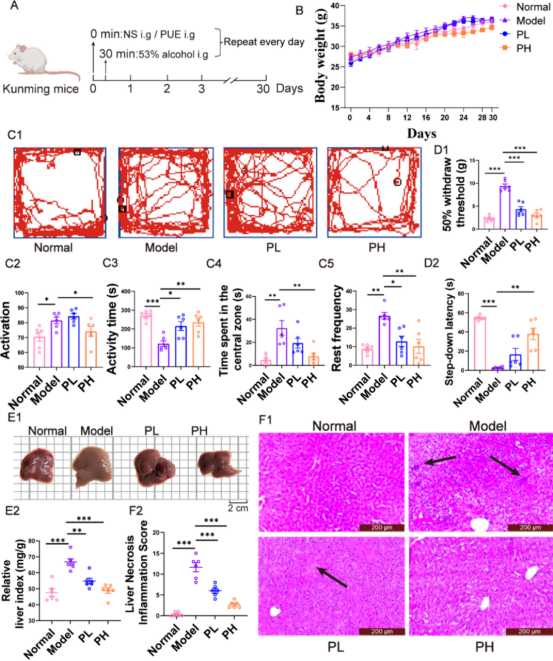
粪便微生物群移植(FMT): 受体小鼠经抗生素处理清除肠道菌群后,分别接受模型组或PUE处理组小鼠的粪便悬液灌胃,同时给予酒精,以验证肠道菌群在PUE治疗ALD中的作用。
行为学测试: 包括翻正反射丧失(LORR)、平衡木实验、爬杆实验、旷场实验、机械痛阈测试和跳台实验。
其他检测: 包括血清生化指标(ALT、AST、TC、TG)、炎症因子(TNF-α、IL-1β、IL-6)和LPS水平、血浆乙醛含量、肝脏和结肠组织病理学(H&E染色)、肠道紧密连接蛋白(ZO-1、occludin)表达、粪便中SCFAs含量测定以及肝脏转录组测序和RT-PCR验证。
讨论与总结
本研究证实,葛根提取物(PUE)通过调节肝-肠-脑轴,对酒精性肝病具有显著的治疗效果。其机制主要包括两个方面:
调节酒精代谢: PUE通过抑制ADH1活性,减少酒精向乙醛的转化,同时激活ALDH2,加速乙醛分解,从而降低体内乙醛蓄积,减轻其对肝脏和肠道的直接毒性。
调节肠道菌群: PUE富集了产SCFAs的有益菌(如拟杆菌属、瘤胃球菌属、普雷沃氏菌属),增加SCFAs水平,从而修复肠道屏障功能,减少LPS渗漏。LPS进入肝脏后,通过TLR4/MyD88/NF-κB信号通路引发的炎症反应也随之被抑制。
此外,PUE还降低了血清炎症因子水平,减轻了由炎症信号通过肠-脑轴传递引起的神经炎症和行为异常。
未来研究
1. 活性成分精准解析
分离鉴定PUE中起关键作用的多糖(2.05 kDa)与异黄酮类成分,探究其协同作用机制,明确“成分-靶点-菌群”的对应关系。
2. 肝-肠-脑轴关键节点验证
利用基因敲除、神经阻断等技术,验证TLR4/MyD88/NF-κB通路及迷走神经在PUE治疗中的核心地位,明确SCFAs作为信号分子的作用。
3. 肠道菌群功能验证
采用无菌动物模型与单一菌定植技术,直接验证关键菌属(如拟杆菌属、瘤胃球菌属)在PUE缓解ALD中的必要性。
4. 临床转化探索
开展小样本临床试验,评估葛根提取物在ALD患者中的有效性与安全性,开发具有辅助保肝、解酒功能的标准化产品。
5. 长期安全性评价
系统评估PUE长期使用的安全性及其对药物代谢酶的影响,为临床应用奠定基础。
文献推荐
IF5.7
Pueraria Extract Ameliorates Alcoholic Liver Disease via the Liver–Gut–Brain Axis: Focus on Restoring the Intestinal Barrier and Inhibiting Alcohol Metabolism

1.YP-Ab-13947/YP-mAb-13947anti-MyD88 antibody
2.anti-NF-κB antibody
3.YP-mAb-18349anti-ZO-1 antibody